Hibridisasi adalah konsep pencampuran orbital atom menjadi orbital hibrida yang sesuai dengan pasangan elektron untuk membentuk ikatan kimia. Orbital hibrida biasanya mempunyai perbedaan energi dan bentuk. Hibridisasi orbital berguna untuk menjelaskan struktur molekuler ketika teori ikatan valensi gagal untuk menjelaskan. Menurut teori hibridisasi, ikatan terjadi akibat terbentuknya orbital hibrida. Orbital Hibrida adalah orbital-orbital yang terbentuk sebagai hasil penggolongan 2 atau lebih orbital atom. Teori hibridisasi dijelaskan berdasarkan penggabungan (hidridisasi) orbital-orbital atom yang digunakan oleh elektron-elektron yang saling berikatan. Teori ini disebut juga teori ikatan valensi.
JENIS-JENIS HIBRIDISASI
A. Orbital sp
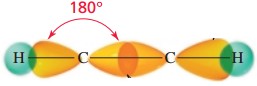
Hibridisasi sp dapat digunakan untuk menjelaskan struktur molekul linier. Bentuk molekul yang dihasilkan hibridisasi sp adalah linear dengan sudut 180o. Orbital 2s dan satu orbital 2p melakukan hibridisasi membentuk dua orbital sp, masing-masing terdiri dari 50% karakter p dan 50% karakter s. Hibridisasi sp merupakan penggabungan antara 1 orbital s dengan 1 orbital p sehingga terdapat 2 orbital p bebas yang tidak digunakan. Hibridisasi sp menghasilkan jenis ikatan rangkap 3 karena terdapat 2 orbital p bebas yang masing masing dapat menghasilkan ikatan phi dengan orbital atom lain sehingga secara keseluruhan hibridisasi ini memiliki 1 ikatan sigma dan 2 ikatan phi. Kekuatan ikatan menjadi kuat lebih kuat daripada dua hibridisasi lainnya dan jarak ikatan juga paling pendek. .
B. Orbital sp2
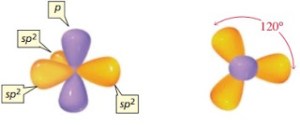
Hibridisasi sp2 merupakan penggabungan 1 orbital s dengan 2 orbital p sehingga terdapat 1 orbital p bebas yang tidak digunakan untuk hibridisasi. Hibridisasi sp2 menghasilkan jenis ikatan rangkap 2 sehingga kekutan ikatannya lebih tinggi daripada ikatan tunggal dan panjang ikatan yang dihasilkan juga lebih pendek. Hibridisasi sp2 berguna untuk menjelaskan bentuk struktur molekul trigonal planar. Orbital 2s dan dua orbital 2p melakukan hibridisasi membentuk tiga orbital sp, masing-masing terdiri dari 67% karakter p dan 33% karakter s. Cuping depan mensejajarkan diri membentuk trigonal (segitiga) planar, menghadap sudut segitiga untuk meminimalisasi penolakan elektron.
C. Orbital sp3
Hibridisasi sp3 dapat menjelaskan struktur molekul tetrahedral. Orbital 2s dan tiga orbital 2p melakukan hibridisasi untuk membentuk empat orbital sp, masing-masing terdiri dari 75% karakter p dan 25% karakter s. Cuping depan mensejajarkan diri dan penolakan elektron bersifat lemah. Hibridisasi satu orbital s dengan tiga orbital p (px, py, dan pz) menghasilkan empat orbital hibrida sp3 yang mempunyai sudut sebesar 109,5º satu sama lain sehingga membentuk geometri tetrahedral. Hibridisasi sp3 memiliki jenis ikatan tunggal atau satu ikatan sigma dimana kekuatan ikatan pada hibridisasi ini paling lemah diantara hibridisasi lainnya, sedangkan panjang ikatan pada hibridisasi ini yang paling besar diantara lainnya.
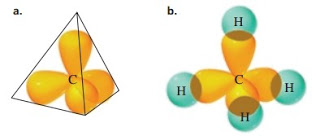
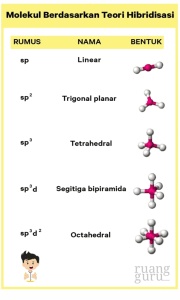
Bentuk molekul berdasarkan teori hibridisasi
LANGKAH-LANGKAH MENENTUKAN HIBRIDISASI
- Menggambarkan diagram elektron valensi atom pusat pada keadaan dasar.
- Menggambarkan kembali diagram orbital namun dalam keadaan tereksitasi sehingga bisa berpasangan dengan elektron dari atom lainnya.
- Menentukan orbital hibrida (orbital baru) dengan melihat orbital-orbital yang terlibat.
PROSES TERJADINYA HIBRIDISASI
Secara keseluruhan, proses hibridisasi terlihat dalam diagram skematik berikut yang mewakili proses hibridisasi atau tingkat hibridisasi yang disertai dengan tingkat energi untuk setiap tahap dan setiap orbital.
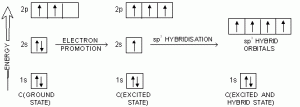
A. Keadaan Dasar (Ground State)
Dalam keadaan dasar, semua atom memiliki konfigurasi elektron yang sama. Dalam keadaan ini, tingkat energi setiap orbital berbeda dan relatif lebih tinggi sehingga kurang stabil.
B. Eksitasi atau Promosi Elektron
Pada tahap eksitasi atau yang juga disebut dengan promosi, salah satu elektron dari orbital 2s di 2p bersemangat ke arah orbital kosong karena masih ada 1 orbital kosong di orbital 2p. Jadi semua orbital 2s dan 2p diisi dengan elektron yang mana 1 elektron diisi.
C. Hibridisasi
Tahap terakhir yaitu hibridisasi atau penggabungan antar orbital di mana di sp3 orbital 2s menghubungkan tiga orbital 3p untuk membentuk sp3 dan seterusnya. Dengan kombinasi ini, tingkat energi yang lebih rendah dan setara diperoleh untuk keempat jenis orbit. Ini menyebabkan panjang ikatan, sudut ikatan, dan energi ikatan menjadi sama.
Tinggalkan komentar