- Perhatikan data hasil percobaan berikut!
| Sifat | Zat P | Zat Q |
| Wujud zat | Padat | Padat |
| Kelarutan dalam air | Larut | Tidak Larut |
| Daya hantar listrik dalam larutannya | Konduktor | Isolator |
| Titik Leleh oC | 750 | -9 |
Berdasarkan data tersebut, jenis ikatan yang terdapat pada zat P dan Q berturut-turut adalah …
a. Logam dan ion
b. Logam dan kovalen polar
c. Ion dan kovalen non polar
d. Logam dan kovalen non polar
e. Kovalen non polar dan kovalen polar
Senyawa P mempunyai wujud padat, dapat larut dalam air, dapat menghantarkan arus listrik dalam larutannya dan dapat memiliki titik leleh tinggi. Dengan demikian senyawa P memiliki ikatan ion. Senyawa Q mempunyai wujud padat, tidak larut dalam air, tidak dapat menghantarkan arus listrik, dan titik leleh rendah. Dengan demikian senyawa Q memiliki ikatan kovalen non polar. Sehingga jawaban yang tepat adalah C.
2. Konfigurasi elektron unsur S dan F berturut-turut adalah :
S = 1s2 2s2 2p6 3s2 3p4
F = 1s2 2s2 2p5
Jika S dan F berikatan membentuk senyawa SF4 , maka bentuk molekulnya adalah ….
a. Tertrahedral terdistorsi
b. Piramida segitiga
c. Piramida segiempat
d. Bipiramida segiempat
e. Huruf T
Atom S dan F saling membutuhkan elektron, maka terjadi pemakaian bersama pasangan elektron (berikatan kovalen) sehingga membentuk senyawa SF4.
Untuk menentukan bentuk molekul dapat menggunakan teori domain elektron.
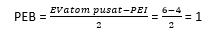
SF4 memiliki 4 PEI dan 1 PEB sehingga bentuk molekulnya tetrahedral terdistorsi.
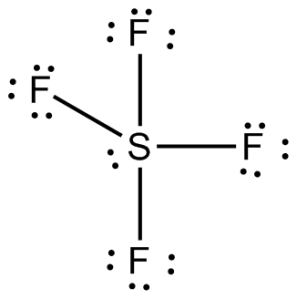
3. Molekul SF6 mempunyai bentuk oktahedral. Jika diketahui nomor atom S = 16, bentuk orbital hibrida SF6 adalah ….
a. sp
b. sp2
c. sp3
d. sp3d
e. sp3d2
Molekul SF6 mempunyai bentuk oktahedral. Dalam molekul SF6 yang menjadi :
Atom pusat = S (nomor atom 16)
Konfigurasi S = 1s2 2s2 2p6 3s2 3p4
Atom S akan berikatan tunggal dengan F(nomor atom 9), karena jumlah elektron valensi F adalah 7 sehingga hanya membutuhkan satu buah elektron lagi agar stabil secara oktet.
Konfigurasi F = 1s2 2s2 2p5
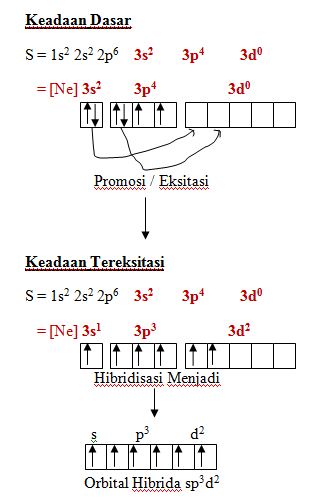
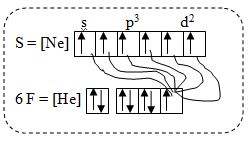
Sehingga jawaban yang tepat adalah E yaitu sp3d2
4. Ramalkan bentuk molekul BeF2!
Dalam molekul BeF2atom pusat Be mengikat 2 atom F.
4Be = 2,2 (Elektron valensi = 2 semua digunakan untuk ikatan)
9F = 2,7 (Elektron valensi = 7 satu elektron digunakan untuk ikatan)
Untuk molekul BeF2 = Jumlah electron valensi Be = 2.
Jumlah electron dari 2 atom F = 2 Jumlah electron = 4
Jumlah pasangan electron = 2
Jumlah pasangan electron ikatan = 2
Bentuk molekul BeF2 adalah linier.

5. Ramalkan kepolaran senyawa NH3 !
Bentuk molekul NH3 adalah trigonal piramida, atom N lebih elektronegatif dari atom H. maka ikatan N-H adalah polar. Oleh karena bentuk NH3 trigonal piramida dan ikatan N-H yang polar mengarah ke atas pusat N maka momen dipolnya tidak sama dengan 0 sehingga bersifat polar. 4. P (nomor atom =15) konfigurasi elektronnya sama dengan [Ne] 3s2 3p3 Supaya dapat membentuk 5 ikatan kovalen, Maka satu electron dari orbital 3s harus dipromosikan ke orbital 3d. selanjutnya orbital 3s, 3orbital 3p, dan 1 orbital 3d mengalami hibridisasi membentuk orbital hibrida sp3d yang berbentuk bipiramida trigonal.
Tinggalkan komentar