Pada ikatan kovalen tidak dikenal kutub positif dan kutub negatif, tetapi ikatan kovalen dapat tertarik oleh medan listrik. Terjadinya kutub listrik dalam ikatan kovalen dikarenakan adanya polarisasi ikatan, yaitu peristiwa yang terjadi akibat adanya perbedaan kekuatan gaya tarik terhadap pasangan elektron yang digunakan bersama. Besarnya kekuatan gaya tarik elektron dari suatu atom dinyatakan sebagai harga keelektronegatifan.
Ikatan kovalen polar adalah ikatan yang pasangan elektron ikatannya cenderung tertarik ke salah satu atom yang berikatan. Ikatan kovalen polar terbentuk antara atom-atom unsur yang memiliki perbedaan nilai keelektronegatifan yang relatif besar. Semakin besar perbedaan harga keelektronegatifan antara kedua atom yang berikatan, maka akan semakin polar ikatannya. Contoh senyawa polar yaitu HCl, HBr, HF, HI, H2O dan NH3.
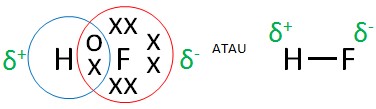
Pada senyawa HF, elektron bersamanya digunakan secara tidak seimbang oleh kedua inti atom H dan inti atom F. HF termasuk molekul polar karena pada molekul H-F, keelektronegatifan F lebih besar dibandingkan H, sehingga elektron cenderung tertarik ke arah F.
Ikatan kovalen nonpolar adalah ikatan yang pasangan elektron ikatannya tertarik sama kuat ke arah atom-atom yang berikatan. Ikatan kovalen nonpolar terbentuk antara atom-atom unsur yang memiliki perbedaan nilai keelektronegatifan yang kecil atau sama dengan nol serta tidak memiliki pasangan elektron ikatan. Contoh ikatan kovalen non polar yaitu H2, I2, Cl2, N2, CH4, O2, BF3 dan C6H6.
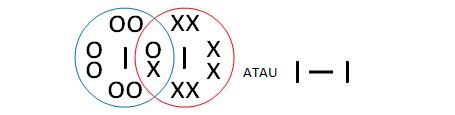
Pada molekul I2 pasangan elektron ikatan tertarik sama kuat ke arah atom-atom yang berikatan. Hal ini dikarenakan antara dua atom I memiliki keelektronegatifan yang sama besar atau dengan kata lain perbedaan elektronegativitas adalah nol. Karena PEI tertarik sama kuat, maka bentuk molekul pada senyawa I2 adalah simetris.
Tinggalkan komentar